À mi-chemin des certitudes
Florence Ader Unité 1111 Inserm / CNRS / ENS de Lyon / Université Claude-Bernard-Lyon
Dès le début de la pandémie de Covid-19, l’OMS a lancé Solidarity, un vaste essai clinique qui rassemble un consortium international. Il inclut Discovery, l’essai européen promu par l’Inserm et piloté par Florence Ader, Prix Recherche Inserm 2020, du Centre international de recherche en infectiologie à Lyon. Son objectif : évaluer, par rapport à une prise en charge standard optimisée, quatre traitements – le
remdesivir, l’hydroxychloroquine, la combinaison lopinavir/ritonavir et cette combinaison associée à l’interféron bêta-1a – déjà administrés dans d’autres maladies pour leur activité antivirale. Selon les résultats intermédiaires, aucun traitement n’a diminué significativement la mortalité globale, le risque d’avoir recours à la ventilation mécanique et la durée d’hospitalisation. Ces précieuses données permettent enfin de se prononcer avec confiance sur les effets – longtemps restés incertains – de ces médicaments. À présent, il est prévu d’évaluer une combinaison d’anticorps monoclonaux, notamment à travers l’essai Discovery.
Au total, Solidarity a inclus 11 330 patients adultes dans 405 hôpitaux répartis dans 30 pays.
Aux prises avec une inflammation dévastatrice
Éric Vivier Unité 1104 Inserm/CNRS/Aix-Marseille Université
Une inflammation hors de contrôle serait à l’origine des formes de la Covid-19 les plus sévères. Selon l’étude Explore Covid-19, soutenue par la fédération hospitalo-universitaire Marseille Immunopole, et coordonnée par Éric Vivier du Centre d’immunologie de Marseille Luminy et d’Innate Pharma SA, cet emballement trouverait notamment son origine dans la surexpression de C5a, une petite protéine aux activités troubles : elle attire et active en grand nombre des globules blancs – neutrophiles, macrophages, monocytes – dotés de son récepteur, C5aR1. Or, ce dernier produit des molécules inflammatoires en masse, les cytokines. Grâce à l’avdoralimab, un anticorps monoclonal développé par Innate Pharma SA qui bloque les récepteurs C5aR1, les chercheurs ont réussi à diminuer l’inflammation chez des souris génétiquement modifiées pour présenter ces récepteurs, normalement réservés aux humains. Ce traitement est maintenant évalué chez des malades qui souffrent de la Covid-19 avec une pneumonie sévère ou un syndrome de détresse respiratoire aiguë.
Un anticorps monoclonal est synthétisé en laboratoire par une lignée de cellules toutes identiques et reconnaît un seul antigène.
Quand le manque d’interféron 1 se fait sentir
Benjamin Terrier Unité 970 Inserm/Université Paris Descartes, Paris-Centre de recherche cardiovasculaire (Parcc)
Qu’est-ce qui caractérise les malades de la Covid-19 à risque de développer des formes sévères ? Un déficit d’activité des interférons de type 1, ont répondu Benjamin Terrier de l’hôpital Cochin à Paris et ses collègues de l’institut Imagine, de l’institut Pasteur et de l’Université de Paris. Au cours de leur étude, les chercheurs ont observé que chez les malades qui présentent des formes légères ou modérées de la maladie, les taux de ces molécules antivirales sont élevés, tandis que chez ceux plus sévèrement atteints, ils sont très bas et semblent chuter très vite après l’infection. Enfin, ils sont encore plus faibles chez les patients en état critique. Ce déficit pourrait donc expliquer en partie les formes graves et, surtout, il constitue un indicateur à surveiller afin d’anticiper l’évolution de la Covid-19. Enfin, des pistes thérapeutiques pourraient émerger dans la mesure où il existe déjà des médicaments capables de pallier cette carence.
Les formes graves de la Covid-19 ressemblent à la vasculopathie de l’enfant associée au gène STING ou SAVI, une maladie génétique rare, responsable d’atteintes pulmonaires.
La grande trahison des gènes
Jean-Laurent Casanova, Laurent Abel Unité 1163 Inserm / Université de Paris ; Université Rockefeller New York / Institut médical Howard Hughes, New York
Formes asymptomatiques, bénignes, sévères ou létales : nous ne sommes pas tous égaux face à la Covid-19. Une des raisons de cette disparité : des profils génétiques et immunologiques spécifiques, identifiés par le consortium international COVID Human Genetic Effort, codirigé par Jean-Laurent Casanova, Grand Prix Inserm 2016, et Laurent Abel de l’institut Imagine à Paris. Certains malades qui développent une forme sévère (3 à 4 %) présentent des anomalies dans 13 gènes impliqués dans la production des interférons de type 1
(IFN 1), des molécules qui constituent la première barrière antivirale. D’autres (10 à 11 %) produisent des auto-anticorps – c’est-à-dire des anticorps qui attaquent l’organisme dont ils sont issus – dirigés contre ces mêmes molécules. Cette production pourrait, elle aussi, être d’origine génétique. Éliminer du sang les auto-anticorps ou compenser la sous-production d’IFN 1 avec des médicaments adaptés, voilà qui pourrait permettre d’éviter la survenue d’une forme grave de la Covid-19 chez les personnes prédisposées.
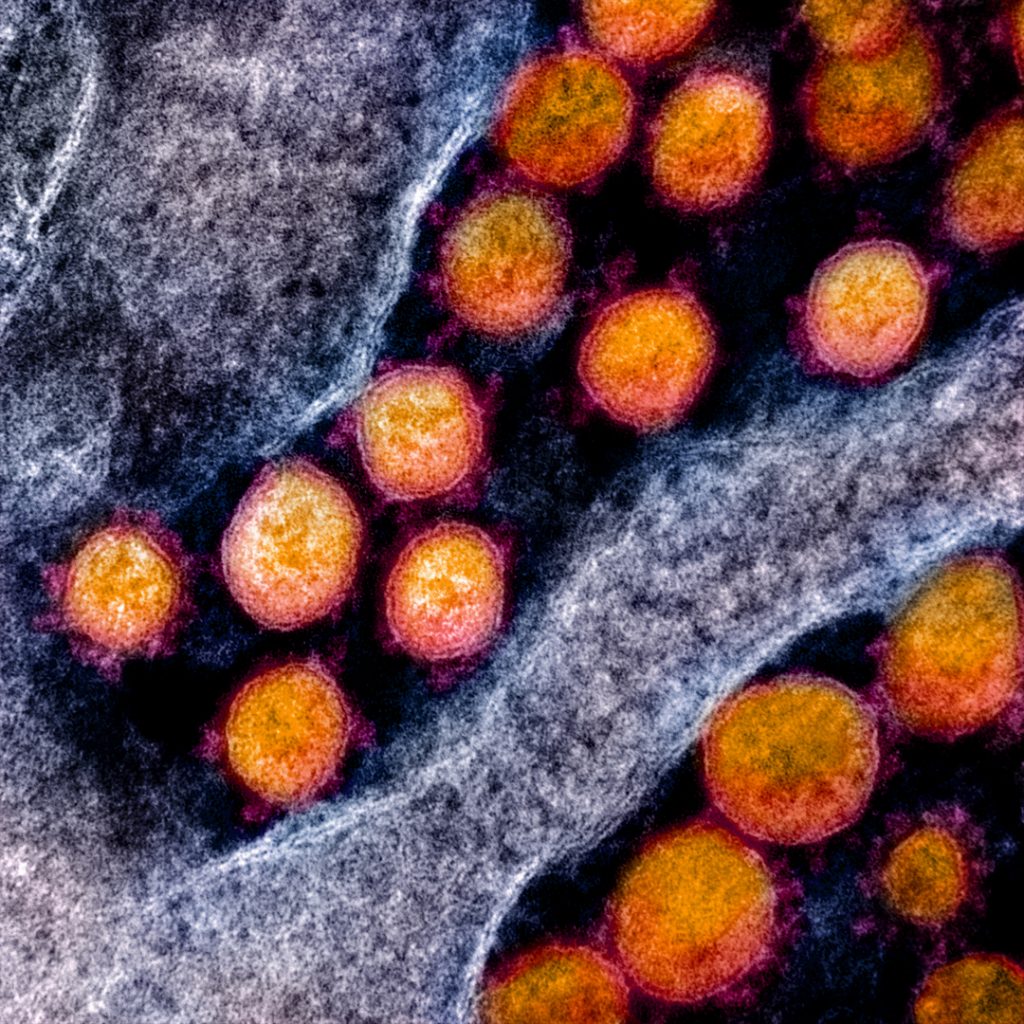
microscopie électronique © NIH
Parmi les malades qui ont des anticorps anti-IFN 1, 95 % sont des hommes, et plus de la moitié a plus de 65 ans.
Persévérer ou s’adapter
Étienne Koechlin Unité 960 Inserm/ENS, Laboratoire de neurosciences cognitives et computationnelles
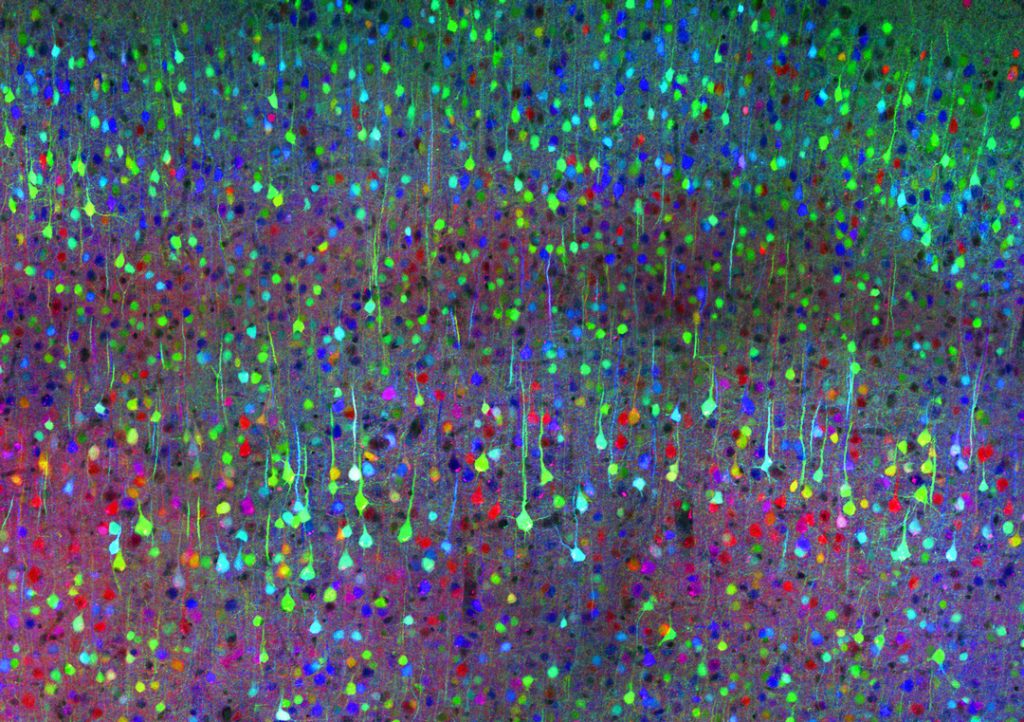
Dois-je m’obstiner à essayer d’enfoncer ce clou à l’aide d’un marteau, ou ferais-je mieux d’opter pour une vis et une perceuse ? Ce genre de situation, en sciences cognitives, est appelé « dilemme exploitation/ exploration ». Dans le cas de l’exploitation, on persiste sur la même voie en tentant d’améliorer sa performance. Dans celui de l’exploration, on change carrément de stratégie. Des travaux dirigés par Étienne Koechlin, chercheur à l’ENS à Paris, ont montré que ce mécanisme se décompose en deux étapes observables au niveau des lobes frontaux. La première, prospective, consiste à évaluer l’action à venir par anticipation, en déterminant les options possibles : il faudra soit persévérer et s’améliorer, soit changer d’approche. La deuxième est rétroactive : elle lit le résultat de l’action qui vient d’être réalisée, interprète son efficacité en fonction du cadre fixé à l’étape précédente, et oriente le comportement vers l’amélioration ou l’exploration. La capacité à résoudre ce type de dilemme est l’une des opérations clés chez les animaux pour s’adapter à un environnement ouvert et changeant, et donc survivre.
Ces données ont été collectées chez des sujets épileptiques, grâce à des électrodes implantées en profondeur dans le cerveau – une technique régulièrement utilisée dans le traitement de l’épilepsie.
Le silence avant les symptômes
Sandrine Humbert Unité 1216 Inserm/Université Grenoble Alpes
La maladie de Huntington est une maladie génétique et
neurodégénérative qui se déclare à l’âge adulte. Pourtant, les premiers signes interviennent très tôt. C’est ce qu’ont montré les travaux dirigés par Sandrine Humbert, chercheuse au Grenoble Institut des neurosciences : la mutation à l’origine de la maladie induit des anomalies dès le stade fœtal. En observant les tissus de fœtus touchés par ces altérations génétiques, la chercheuse et son équipe ont découvert que la huntingtine, la protéine affectée par la mutation, n’est pas située au bon endroit dans les populations de cellules destinées à former, plus tard, les neurones du cortex. Ce phénomène affecte la formation du cil de ces cellules, essentiel au bon développement des neurones. En outre, la division et le cycle cellulaires sont perturbés. Ces observations ont été confirmées chez des modèles de souris. La maladie de Huntington altère profondément le développement neurologique, et pourtant, chose fascinante, le cerveau arrive à compenser ce déficit et à le rendre invisible pendant des dizaines d’années.
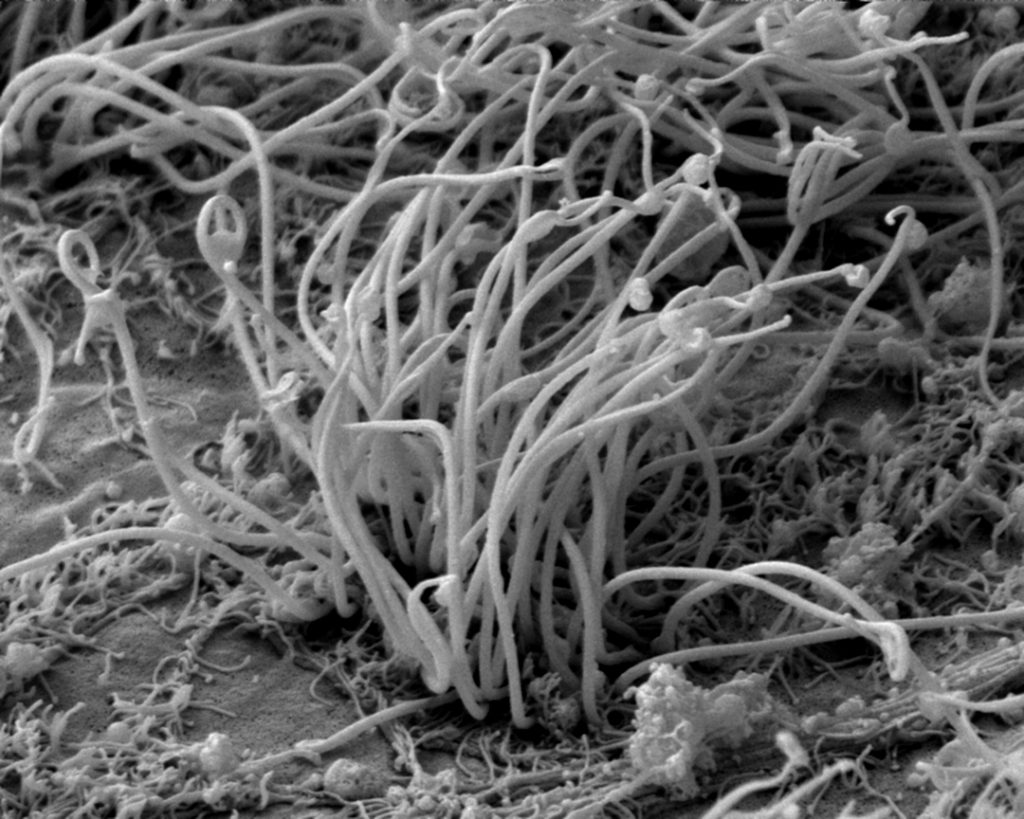
Presque toutes nos cellules possèdent un cil primaire. Dans notre cerveau, cette sorte d’antenne est essentielle au développement neurologique.
Sandrine Humbert
L’oubli, meilleure réponse au traumatisme ?
Pierre Gagnepain Unité 1077 Inserm/EPHE/Unicaen, Neuropsychologie et imagerie de la mémoire humaine
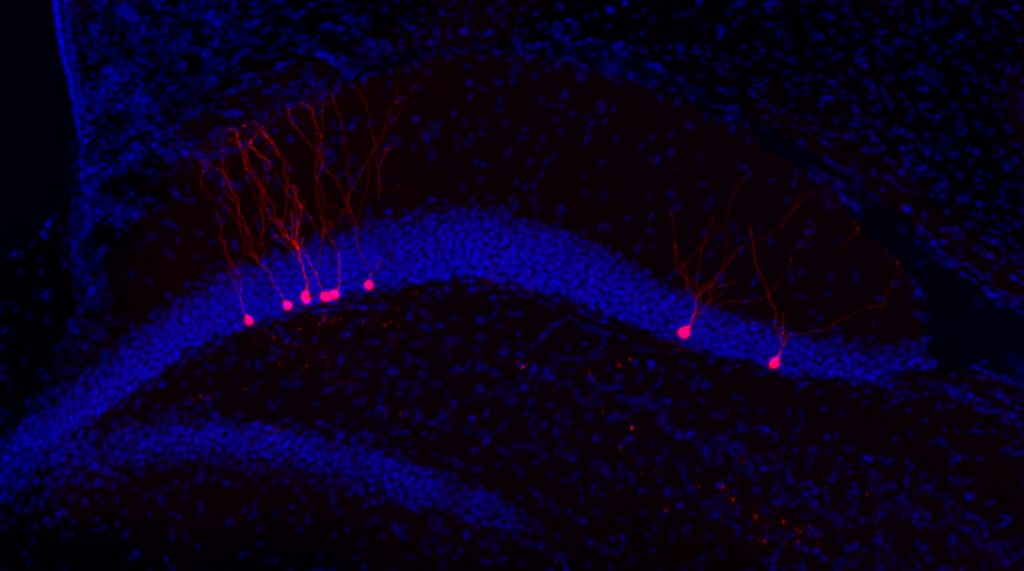
cérébrale indispensable aux phénomènes de
mémorisation © Inserm / Ariane Sharif
Les souvenirs des attentats du 13 novembre 2015 n’ont pas le même impact émotionnel chez tous les survivants de ces événements tragiques. Certains réussissent à se reconstruire, d’autres développent un trouble de stress post-traumatique (TSPT). Chez ces derniers, les souvenirs effrayants surgissent fréquemment, de manière intrusive, et s’accompagnent d’émotions très fortes qui peuvent être vecteur d’isolement social. Jusqu’ici, on associait ce phénomène à un trouble
de la mémoire qui empêche la bonne intégration du souvenir traumatique. Mais les travaux de Pierre Gagnepain et de son équipe de l’université de Normandie à Caen montrent également l’existence d’un dysfonctionnement du mécanisme de suppression des souvenirs, impliqué notamment dans ce qu’on appelle l’« oubli actif ». Ces résultats ont été obtenus grâce à l’imagerie cérébrale de survivants des attentats de 2015, certains souffrant de TSPT, d’autres non, pendant qu’ils réalisaient une tâche d’inhibition d’images intrusives. Ils ouvrent la voie à de nouveaux traitements qui cibleraient ces mécanismes de contrôle favorisant la résilience et l’oubli.
Le programme de recherche 13-Novembre, dont l’Inserm est cofondateur et qui est intégré à l’étude Remember sur le TSPT, a été lancé après les
attentats.
Quand les interactions sociales partent en fumée
Giovanni Marsicano Unité 1215 Inserm/Université de Bordeaux
En dépit de sa popularité dans un cadre festif, le cannabis affecte bel et bien les comportements sociaux. Les mécanismes sous-jacents ont été révélés par une équipe de chercheurs dirigée par Giovanni Marsicano, du Neurocentre Magendie de Bordeaux, et Juan Bolaños, de l’université de Salamanque en Espagne. Les neurones fonctionnent grâce à l’énergie apportée par d’autres cellules, les astrocytes. Ces derniers ont pour mission d’extraire le glucose de la circulation sanguine et de le transformer en énergie, dont le cerveau tirera partie afin de moduler les comportements de manière appropriée. Lors de leurs expériences, les chercheurs ont exposé des
souris au delta-9-tétrahydrocannabinol, ou THC, principal composant psychoactif du cannabis. Or, ils ont observé que le THC se fixait à des récepteurs situés sur la membrane des mitochondries des astrocytes. Cette fixation entraînait une altération de production d’énergie et donc du fonctionnement des neurones. En conséquence, les comportements sociaux sont altérés, et ce jusqu’à 24 heures après l’exposition. À l’heure où l’utilisation du cannabis à des fins thérapeutiques est à l’étude, ces résultats devront être pris en considération.
© Inserm / Yasmina Saoudi
Les astrocytes sont ainsi nommés parce qu’ils arborent une forme d’étoile.
La semaine prochaine : « Au cœur du vivant ». Rendez-vous pour huit nouveaux faits scientifiques marquants de 2020 !
Retrouvez toutes les avancées scientifiques du rapport d’activité 2020 de l’Inserm :