Projet Pediacircaroma
Le projet Pediacircaroma de Loélia Babin, se concentre sur les taux de rechutes importants après traitement du lymphome pédiatrique. Son projet explore l’implication d’une classe d’ARN circulaire dans la résistance au traitement.
Le lymphome anaplasique à grandes cellules (ALCL) est un cancer du système immunitaire qui affecte principalement les enfants et les adolescents, caractérisé par une anomalie génétique (NPM-ALK). Bien que 75% des patients répondent bien à la chimiothérapie, la résistance au traitement conduit à un taux de mortalité élevé. Comprendre les mécanismes de résistance est crucial pour identifier de nouveaux biomarqueurs et cibles thérapeutiques.
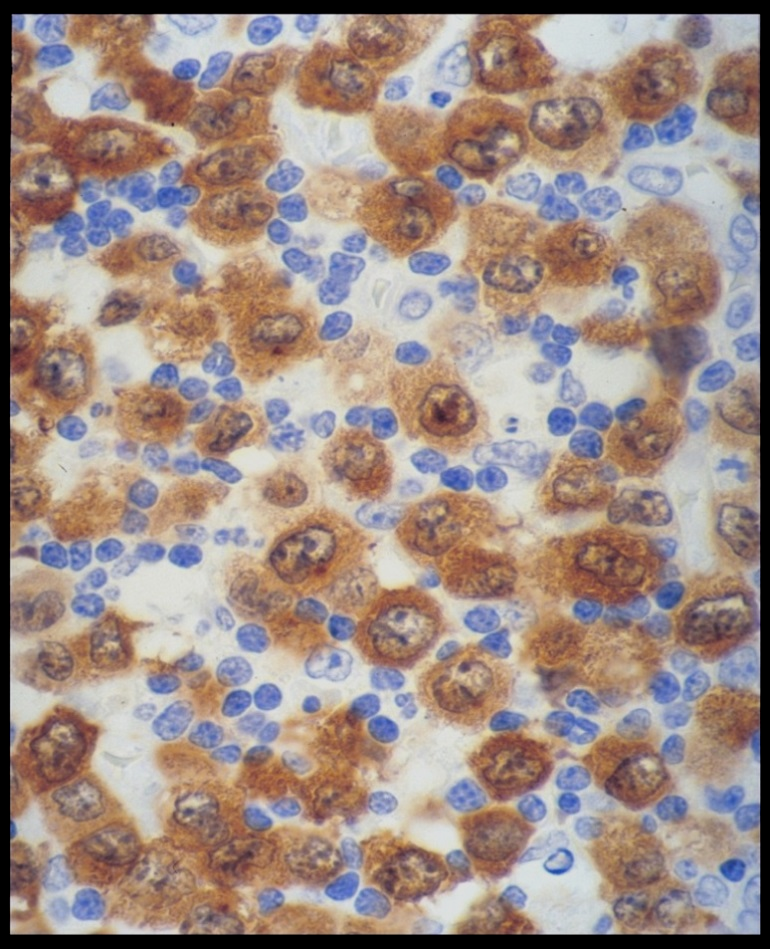
Des recherches récentes ont mis en évidence le rôle des ARN circulaires dans les cancers. Ces ARN peuvent être détectés de manière peu invasive dans le sang des patients. Le projet de recherche vise à identifier les ARN circulaires spécifiques aux patients atteints d’ALCL et à comprendre leur rôle dans la maladie et la résistance aux traitements.
Dans notre laboratoire, nous avons identifié différents ARN circulaires associés à l’anomalie génétique NPM-ALK. Notamment, nous avons pu montrer que l’un des ARN circulaires est présent dans le sang des patients ALCL mais absent chez les individus sains, faisant de lui un biomarqueur potentiel. La présence de cet ARN circulaire est liée à une diminution de l’efficacité d’un traitement clinique. Réduire la quantité de cet ARN dans les cellules dérivées des patients améliore la réponse au traitement, suggérant qu’il pourrait être une nouvelle cible thérapeutique.
Le laboratoire collabore avec une équipe de recherche pour développer des molécules capables de détruire spécifiquement cet ARN circulaire, espérant ainsi améliorer la réponse aux traitements et offrir une nouvelle stratégie pour combattre la résistance, augmentant l’efficacité des thérapies et offrant un nouvel espoir aux patients.
Projet Disrupt
Le projet Disrupt de Jean Cacheux, propose de revisiter l’injection intratumorale grâce à la technologie des « tumeurs sur puce ». Ce projet vise à optimiser la biodistribution des médicaments dans les tumeurs pancréatiques, améliorant ainsi l’efficacité des traitements actuels.

Le cancer du pancréas est l’une des principales causes de décès par cancer, souvent diagnostiqué à un stade avancé avec des options de traitement limitées. Bien que la chirurgie puisse offrir un espoir de guérison, les résultats demeurent incertains, même en combinaison avec la chimiothérapie.
Au Centre de recherche en cancérologie de Toulouse, l’équipe ImPact est spécialiste dans la thérapie génique et les virus oncolytiques, des virus capables de cibler et de détruire les tumeurs. Cependant, améliorer l’accessibilité de ces virus aux cellules cancéreuses reste un défi majeur, car les tumeurs pancréatiques sont particulièrement résistantes.
Pour surmonter ce défi, nous proposons d’optimiser les injections locales en utilisant des principes biophysiques afin de franchir les barrières physiques de l’écosystème tumoral. Nous allons utiliser des dispositifs de type « tumeur sur puce », développés en collaboration avec le LAAS-CNRS et basés sur des techniques avancées d’impression 3D et de découpe laser. Cette technologie nous permettra de recréer les conditions d’une tumeur pancréatique en laboratoire et d’étudier comment différents paramètres d’injection influencent la distribution des virus oncolytiques.
Ce projet interdisciplinaire établit un lien entre la physique, la biologie et l’oncologie, répondant à un besoin crucial dans le traitement du cancer. Des résultats positifs pourraient révolutionner la thérapie du cancer en améliorant la distribution des agents thérapeutiques, avec des applications potentielles pour d’autres types de cancers également.



